臨床研究對象(受試者)保護中心
目的
為保障臨床研究對象(受試者)之安全、權益與福祉,設立「研究對象(受試者)保護中心」,透過與本院「人體試驗委員會」之合作,整合「醫學研究部臨床試驗中心」、「臨床試驗藥局」等單位,制定本院研究對象(受試者)保護計畫,提升對全院研究對象(受試者)之保護與臨床研究品質。
範圍
凡符合人體研究法第4條所定義之人體研究(指從事、取得、調查、分析、運用人體檢體或個人之生物行為、生理、遺傳、醫學等有關資訊之研究);其有關於受試者權益與安全保護之相關業務及受試者正確之人體研究觀念與與推廣均為本中心業務範圍
權責
1. 本中心之任務為臨床研究受試者保護業務之統合、協調、管理與監督
1.1 監督本院人體試驗委員會行政作業,以及研究人員之臨床研究受試者保護相關業務
2.1 監督研究合約之審查
3.1 監督臨床研究受試者保護之教育訓練
2. 臨床研究受試者保護之稽核與品質改善。
3. 臨床研究受試者保護諮議委員會之會務運作。
4. 受理人體研究之受試者、研究人員以及其他人士,對臨床研究受試者保護相關業務之諮詢、申訴或建議。
5. 支援臨床研究受試者保護諮詢委員會行政業務。
6. 舉辦民眾教育訓練宣導活動,傳達臨床試驗相關知識,提升民眾正確之臨床試驗觀念。
7. 針對在本院執行之各種人體研究,核對相關文件,代表機構同意研究可在本院執行。
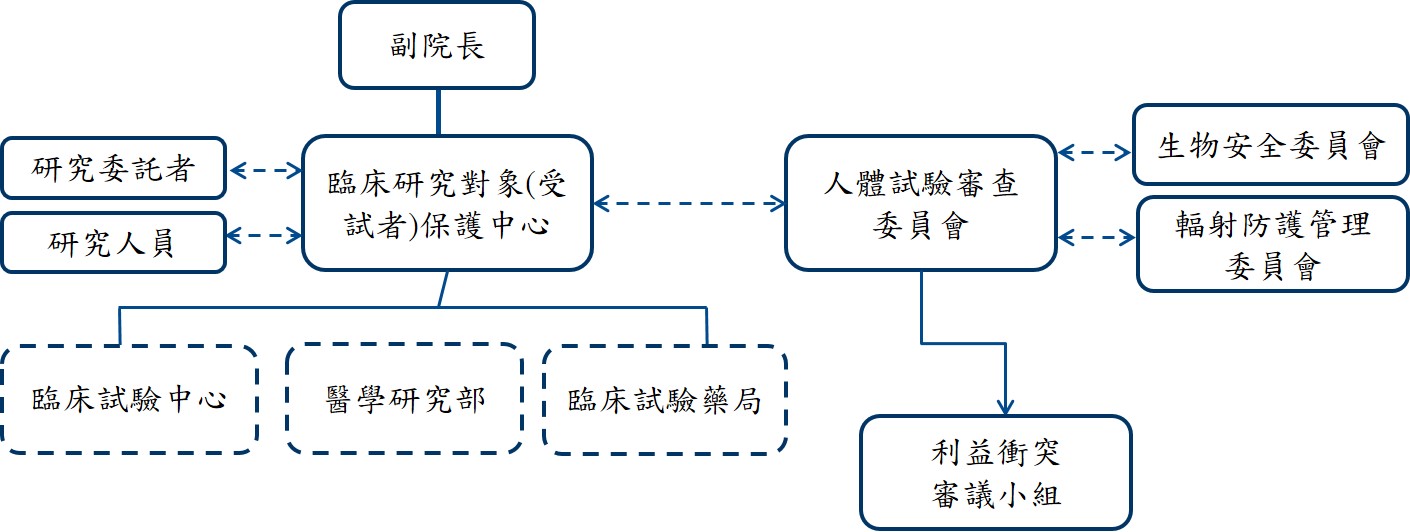
本院設有研究機構、受試者保護中心與審查會之權責分工組織圖。督導受試者保護工作,各研究機構具適當的授權及獨立性。
試驗不是非參加不可,因此參加試驗前需先知道:
| 1、這個試驗的目的是什麼? | 研究的目的是增加知識。因此應該要知道,此試驗是在探索那些方面的知識。研究人員應該用通俗易懂的話,讓我們受試者知道這個試驗的目的是什麼,是不是非參加不可。若不參加,還可以接受什麼治療方法。 |
| 2、試驗過程將發生什麼事? | 需知道試驗過程要在你身上做那些事,該怎麼配合(例如隔多久要回診一次?每次要抽多少血?做什麼檢查?),會帶給生活多少不便(例如不能開車,需避孕)。 |
| 3、可能會發生什麼不良反應? | 任何試驗一定有風險,因此需知道參加此試驗的危險性有多大。務必問清楚在既有的資料中,可能發生什麼副作用及其發生率,最好能確切掌握發生率的數字。同時,也務必了解萬一發生危險或緊急狀況時,該怎麼辦?和誰聯絡? 如何聯絡?以及誰會提供後續醫療救治? 還有相關費用問題。在加入試驗前都應仔細問清楚。 |
| 4、試驗對我個人的好處及預期效果? | 試驗不是非參加不可,因此參加試驗之前需好好考慮。參加試驗之前要考慮「研究」不一定對你個人有幫助。「治療」是已經證明有效的處置,因此會對接受者有益處。但「試驗」是還不確切知道會發生怎樣的結果,因此試驗不一定對參加者有幫助。但試驗結果可能會幫助和你有同樣健康問題的人。因此需好好考慮是否願意參加,也需知道預期效果有多大,才不會有過於樂觀的不當期待。 |
| 5、不參加試驗有沒有其他治療方法? | 試驗不是非參加不可,因此需要知道是否還有其他治療方法?或是參加試驗是唯一嘗試新治療方法的機會。 |


諮詢窗口:
信箱:hrpc@cgh.org.tw
電話:(02)27082121-6990
更新時間:2026/1/16